Therapie - Tumororthopaedie
Hauptmenü
- Tumororthopädie
- Aktuelles
- Ärzteinfo
-
Knochensarkome
- Knochensarkome
- Knochensarkomtypen
- Weichteilsarkome
-
Gutartige Tumoren
- Übersicht
- Knochenbildend
- Knorpelbildend
- Riesenzelltumor
- Tumorähnliche Läsionen
- Multiples Myelom
-
Metastasen
- Übersicht
- Einzelne Karzinome
-
Operative Therapie
- Biopsie
- Resektion
- Knochentransplantation
- Tumorendoprothetik
- Kürettagen und Auffüllung
- Beckenresektionen
- Wirbelsäuleneingriffe
- Amputation
- Umkehrplastik
- Nachsorge
- Team
- Publikationen
- Terminvereinbarung
- Anfahrtsweg
- Befundzusendung
- Zweitmeinung
- Internetforen Selbsthilfegruppen
- Kontakt
- Impressum
Therapie
Zusammenfassung
Prinzipiell sollte bei der Therapie von nicht metastasierten Weichteilsarkomen eine vollständige Entfernung im gesunden (R0-
Prinzipielles Vorgehen
Ziel der Resektion ist die kompartmentorientierte (intrakompartmentale Lokalisation) oder die weite Resektion (extrakompartmentale Lokalisation). Konzepte der prinzipiellen, vergleichsweise sehr aggressiven Kompartmentresektionen der 1980er-
Die neoadjuvante Radiotherapie wird mit dem Ziel der lokalen Tumorremission und Verbesserung der Resektabilität eingesetzt. Eine Reduktion des Risikos einer Metastasierung ist bisher nicht belegt. Durch die vor der Operation erfolgte Radiotherapie ist allerdings eine im Vergleich zur adjuvanten (nach der Operation) Radiotherapie gesteigerte Rate von Wundheilungsstörungen zu erwarten. Der Vorteil der neoadjuvanten Radiotherapie liegt im kleineren Zielvolumen (klar definierbare Tumorgröße ohne potenziell kontaminiertes Operationsfeld) und damit in der geringeren Strahlendosis. Aufgrund der doch erheblichen Wundkomplikationen bevorzugen wir am Klinikmum der LMU allerdings im Extremitätenbereich die adjuvante Bestrahlung.
Systemische Chemotherapie
Im Kindesalter ist die systemische Chemotherapie bei der Behandlung der Weichteilsarkome im Rahmen von Therapieoptimierungsstudien bestens etabliert. Im Erwachsenenalter ist die neoadjuvante Che-
Die ILP mit Tumornekrosefaktor alpha und Melphalan hat sich in mehreren klinischen Studien als effektive Induktionstherapie beim lokal fortgeschrittenen und primär nicht extremitätenerhaltend R0-
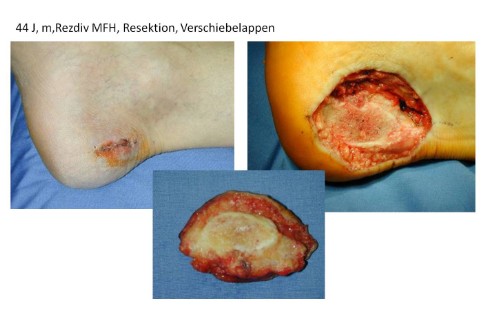
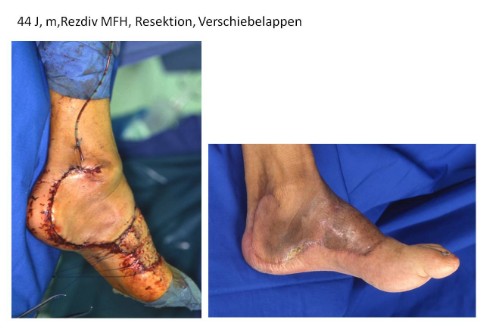
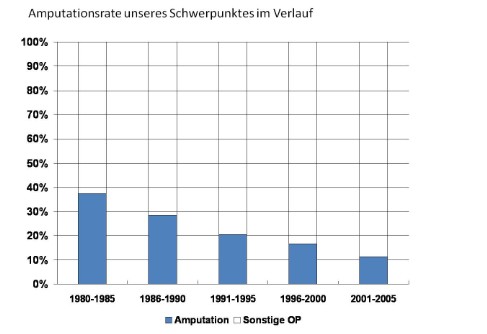
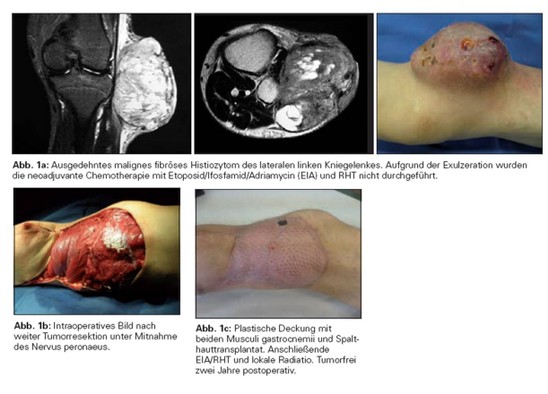
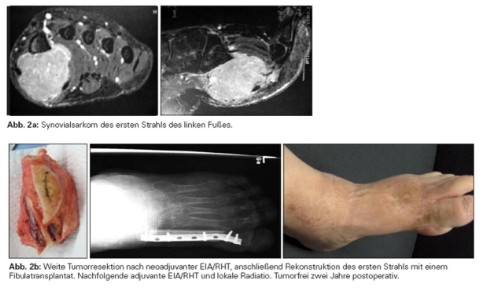
Publizierte Daten über das chirurgische Vorgehen und chirurgische Behandlungsergebnisse nach einer neoadjuvanten Therapie sind Ausnahmen. Die Frage, ob sich das Ausmaß der Tumorresektion in Abhängigkeit vom Ansprechen des Tumors verändert, ist bisher nicht geklärt. Die Indikation zur Amputation sollte nur nach Diskussion aller multimodalen Therapieoptionen und Einholung einer Zweitmeinung gestellt werden, da die Gesamtprognose in der Regel nicht positiv zu beeinflussen ist. Derzeit wird die primär operative Therapie eines Weichteilsarkoms bei etwa 45% der Patienten durchgeführt (Abbildungen 1a bis c), etwa 35% werden neoadjuvant therapiert und anschließend reseziert (Abbildungen 2a und b) und zirka 20% erhalten im primär metastasierten Stadium eine palliative systemische Therapie. Der Anteil extremitätenerhaltender Eingriffe liegt unter Berücksichtigung der vorhandenen multimodalen Therapieansätze bei deutlich mehr als 80%. Im Schwerpunkt Tumororthopädie liegt die Ampuationsrate bei unter 10%. Oft ist die Amputation eher Folge einer Komplikation nach Extremitätenerhalt und aufwendiger Rekonstruktion als durch einen nicht extremitätenerhaltend zu resezierenden Tumor bedingt. Plastisch rekonstruktive Verfahren sind in mehr als 25% der operativ therapierten Weichteilsarkome erforderlich.
Prinzipien der Resektion
Die Tumorresektion ist Standard und Basis der lokalen Tumorkontrolle. Die Behandlungsstrategie wird naturgemäß vom Tumorstadium und der Lokalisation bestimmt. Das definierte Ziel im nicht metastasierten Stadium ist die R0-
Resektion bei verschiedenen Tumorlokalisationen
Peripherer Extremitätenbereich
Bei etwa 25% aller Resektionen von Weichteilsarkomen der Extremitäten sind plastische Rekonstruktionen erforderlich. Diese reichen von lokoregionären Lappen, freien Lappenplastiken, Meshgraft-
Ein Fortschritt ist zum Beispiel die Transposition einer künstlichen Achillessehne, eingebettet in einen Musculus-
Die Infiltration von Gefäßen durch Weichteilsarkome muss nicht mit der Empfehlung zur Amputation einhergehen. Meist handelt es sich um hochmaligne Sarkome, die per se ein höheres Metastasierungsrisiko und eine schlechtere Prognose bedeuten. Durch eine Amputation ist dieses Problem nicht zu lösen. Entsprechend sollte auch hier eine R0-
Die Indikation zur Amputation kann unter kurativer und palliativer Intention gegeben sein. Sie liegt unter kurativer Intention vor, wenn auch unter Einbeziehung weiterer Therapieoptionen (systemische Chemotherapie in Kombination mit RHT, ILP, Radiotherapie) eine R0-
Gerade bei diesen Tumorlokalisationen ist immer eine neoadjuvante Therapie mit dem Ziel der lokalen Remission des Tumors zu erwägen. Die plastisch-
Die Kriterien der operativen Therapie des Lokalrezidivs unterscheiden sich nicht von denen des Primärtumors. In den meisten Fällen liegt aber eine ungünstigere lokale Situation vor. Besonders, wenn es sich um Rezidive im und am Strahlenfeld, nach einer Extremitätenperfusion oder nach vorausgegangenen plastisch-